Ziel der Synthetischen Biologie ist es, künstliche biologische Systeme für Anwendungen in Biotechnologie und Medizin zu entwickeln. Die erfolgreiche Implementierung neuartiger, zellulärer Signalwege erfordert genetische Schalter, die die Expression einzelner Module innerhalb des Signalweges optimieren.
Wir sind daran interessiert, neuartige RNA-basierte Schalter zu entwickeln, deren Funktion durch exogene Liganden gesteuert werden können. Um eine hochspezifische Ligandenerkennung und Orthogonalität zwischen den verwendeten Molekülen zu erreichen, nutzen wir RNA-Aptamere als Sensoreinheiten. RNA-Aptamere sind in vitro selektierte RNA-Moleküle, die, genau wie Antikörper, einen bestimmten Liganden mit hoher Spezifität und Affinität erkennen.
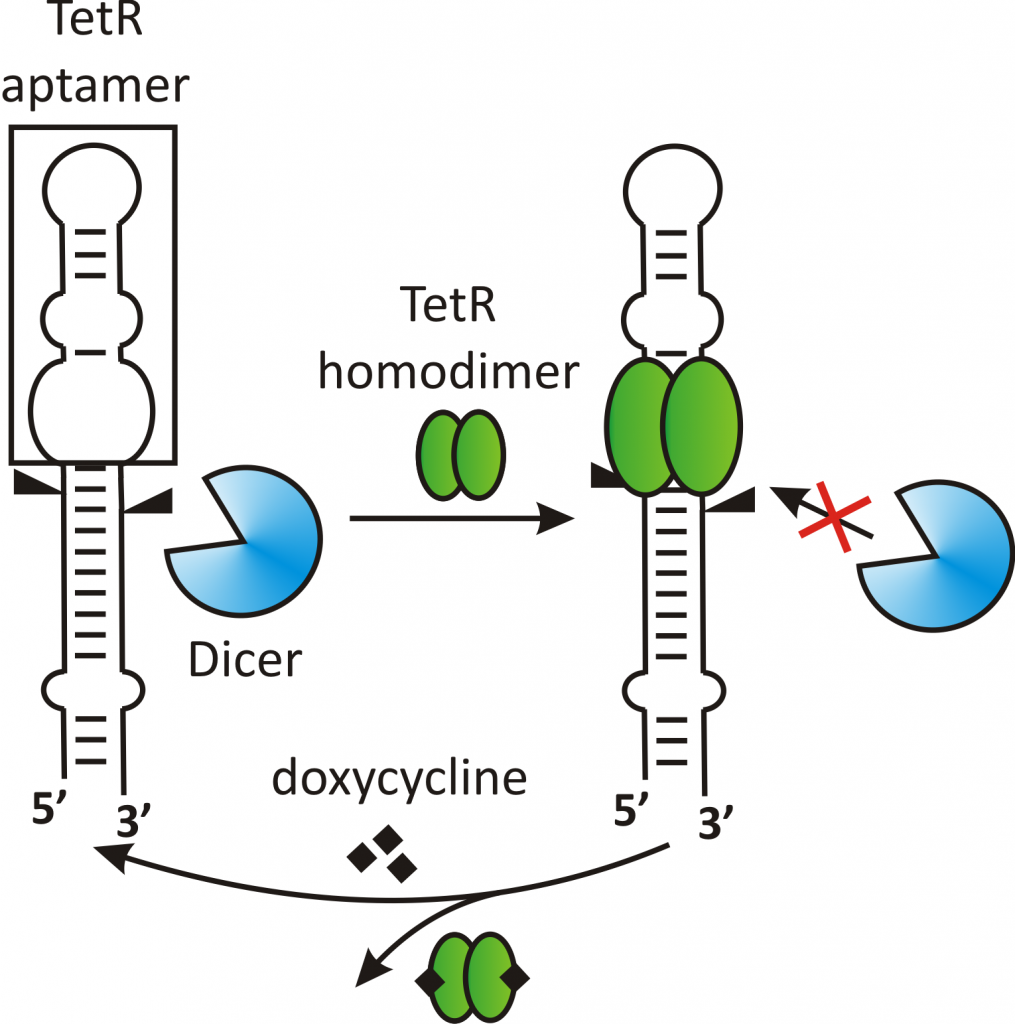
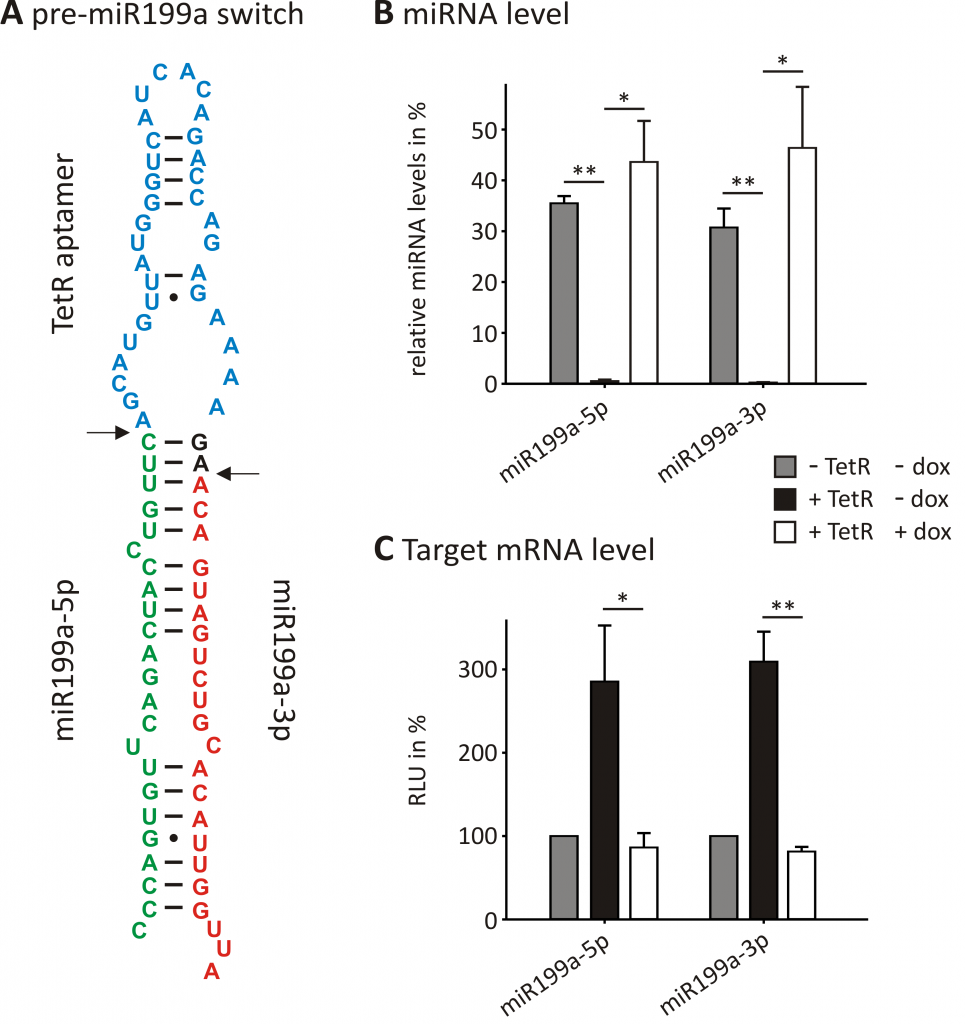
Unter anderen haben wir ein vom bakteriellen Repressor TetR erkanntes Aptamer verwendet, um die Reifung von miRNAs zu kontrollieren (Abb. 1). miRNAs sind kleine, nicht-kodierende RNAs, die die Genexpression unterdrücken, indem sie direkt an die 3’UTRs von mRNAs binden. Die reifen miRNAs werden aus einem langen primären RNA-Transkript in einem zweistufigen Prozess herausgeschnitten. Die Funktionalisierung eines solchen Transkripts mit dem TetR-Aptamer ermöglichte es uns, den zweiten Prozessierungsschritt reversibel zu steuern. Dadurch können wir den Gehalt an miRNA und in Folge den ihrer Ziel-mRNAs in Zellen kontrollieren (Abb. 2). Zukünftig wollen wir unsere neu identifizierten posttranskriptionellen Elemente aus FOKUS 1-3 in genetische Kreisläufe integrieren und damit den Werkzeugkasten der Synthetischen Biologie um neuartige, gut charakterisierte Schalter erweitern.